![]()
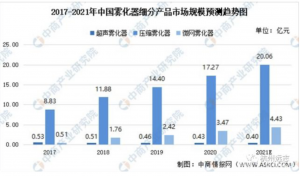
来源:中商情报网
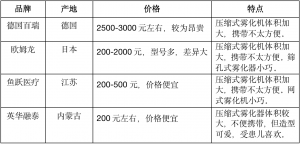
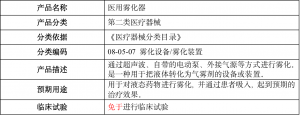
根据2018年8月1日实施的新版《医疗器械分类目录》判定,医用雾化器具体信息如下:
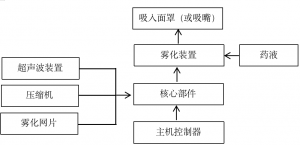
不同雾化器工作原理示意图
![]()
医用雾化器是市面上比较常见的医疗器械,有其行业标准,为YY 0109-2013 医用超声雾化器,以超声雾化器为例列举主要性能指标(压缩雾化器和网式雾化器类似,无实质性差别),产品进行注册时可参考以下指标。
(1)超声振荡频率:雾化器超声工作频率与标称频率的偏差:≤±10%。
(2)最大雾化率:雾化器的最大雾化率必须不小于其企业标准、使用说明书(或铭牌)上的规定。
(3)雾化器水槽内温度:雾化器水糟内水温≤60℃。
(4)整机噪声试验:雾化器正常工作时的整机噪声:≤50dB(A计权)。
(5)雾化率调节性:雾化器的雾化率宜能调节。
(6)低水位提示或停机装置:雾化器宜具备低水位提示或停机装置。
(7)风量调节装置:雾化器宜在适当部位安装风量调节装置。
(8)定时误差:雾化器宜有定时控制装置,其控制时间与标称时间的偏差不大于10%。
(9)连续工作时间:雾化器在常温下,采用交流电源供电时,连续工作4小时以上,应能正常工作;如采用直流电源供电时,连续工作1小时以上,应能正常工作。如申请人在产品技术要求中规定了连续工作时间,则依据产品技术要求的规定。
(10)外观与结构:雾化器外观应整洁,色泽均匀,无伤痕、划痕、裂纹等缺陷。面板上的文字和标志应清晰可见;雾化器塑料件应无气泡、起泡、开裂、变形以及灌注物溢出现象;雾化器的控制和调节机构应安装牢固、可靠,紧固部位应无松动;雾化器的水槽、管道应无泄漏。
(11)安全性能要求:应符合GB 9706.1、YY0505的全部要求。
(12)环境试验:应根据产品特点,在产品技术要求中按GB/T 14710规定气候环境和机械环境试验的组别,并在随机文件中说明。试验时间、恢复时间及检测项目可参考GB/T 14710附录A的内容编写。
(13)雾粒等效体积粒径分布:与实际颗粒具有相同体积的同物质的球形颗粒的直径叫做等效体积粒径。制造商应公布雾化器产生的雾粒等效体积粒径分布曲线,应公布雾粒的中位粒径,其误差应不超过±25%。还应公布测量时雾化的溶液成分和温度、湿度。按照激光散射法或EN13544-1规定的瀑布撞击法检测,等效体积粒径分布应符合制造商的规定。
(14)其他:医用雾化器配件如吸嘴等有单独的性能指标要求。
![]()
医用雾化器的生产工艺流程图如下:
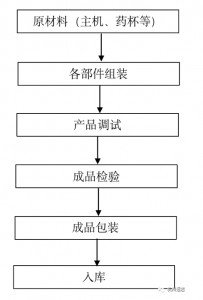
注:以上仅图示大致工艺流程图,具体因不同厂家自定
![]()
